
Juan Nicolás Cuenca
Fisioterapeuta, Hospital Guadarrama, Madrid
Nº Col: 564, Colegio de Fisioterapeutas de Madrid
Diplomatura de Fisioterapia en la Universidad de Cadiz en la promocion 1990-93
Resumen
El aprendizaje motor requiere feedback; cuando una persona está adquiriendo una nueva habilidad, o modificando una habilidad ya adquirida debido a una disfunción física, el feedback sensorial optimiza el aprendizaje motor.
La electromiografía es una disciplina que se ocupa de la evaluación clínica y neurofisiológica de la patología neuromuscular y de ciertos aspectos de la patología del S.N.C. (daño cerebral adquirido, traumatismo cráneo-encefálico, etc…).
Actualmente, el uso de aparatos que operan con este biofeedback, amplificando la señal generada en las placas motoras, ha permitido la introducción de esta herramienta terapéutica en el tratamiento de pacientes con daño cerebral adquirido, proporcionándoles un refuerzo muy útil en la mejora del control motor y de la función deficitaria, permitiéndoles desarrollar sus habilidades sensioromotoras específicas y mejorar el movimiento, no solo de un modo analítico, sino durante una tarea ocupacional; el uso de aparatos portátiles y de fácil manejo ha hecho extensible su uso en el control y mejora funcional de las actividades de la vida diaria
Palabras clave
Biofeedback, electromiografía de superficie, condicionamiento operante, imagen mental, daño cerebral, línea de base, valor umbral, dispersión, actividad tónica, E.P.P. E.M.D. actividad de la vida diaria.
INTRODUCCIÓN
Los sistemas de biofeedback electromiográficos, son dispositivos que permiten ampliar una señal fisiológica, en este caso concreto, la actividad de los músculos monitorizados, presentándola de una forma simple de entender pára el paciente, mediante gráficas, animaciones, sonidos, etc… de este modo se facilita la capacidad del sujeto de controlar voluntariamente su actividad muscular por el hecho de darle información puntual acerca de la misma de una forma proporcional al nivel de ejecución o control de la función.
Las principales teorías propuestas para describir los efectos del entrenamiento con biofeeback se basan en dos modelos fundamentales:
- Modelo del aprendizaje instrumental u operante basado en la importancia del refuerzo y la motivación.
- Modelo del procesamiento de la señal, basado en la importancia de la elaboración de la imagen motora a nivel cortical.
BASES DEL BIOFEEDBACK
Modelo del servomecanismo
Los servomecanismos son sistemas de control que permiten regular una función, en este caso la muscular. Estos sistemas son autoadaptativos, cambian en función de las variaciones del medio, y abiertos, interaccionan con el medio modificando la función según los cambios que se introducen en el sistema; así pués, podemos decir que los sistemas de biofeedback consideran al sistema nervioso del paciente como un servomecanismo abierto muy complejo, donde el dispositivo electrónico proporciona información al sujeto que genera un feedback (fig. 1).
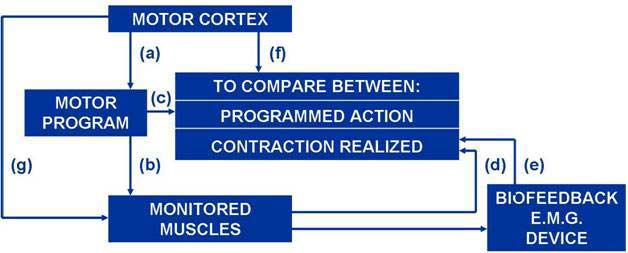
Fig. 1. Control de la contracción con biofeedback con E.M.G. La corteza motora toma una decisión (a) que va al programa motor, donde se da la orden de ejecución (b); en el centro comparador se compara la contracción realizada (d y e) con la programada (c), cuyas diferencias son enviadas a la corteza motora (f), que realiza las correcciones pertinentes.
Procesamiento de la señal en feedback
Se consideran dos tipos de feedback:
- Feedback positivo: La salida (la acción ejecutada) provoca el efecto de aumentar la entrada (fuente de información), provocando un efecto de aceleración que aleja al sistema de la estabilidad.
- Feedback negativo o inhibitorio: La salida provoca una disminución de la entrada, de modo que el sistema recupera el equilibrio.
La propiocepción es una fuente esencial de feedback sensorial, siendo también importante la información visual, auditiva y táctil; por eso, cualquier déficit en el flujo o la organización aferente sensorial (propioceptiva y exteroceptiva) producirá una alteración en la ejecución del patrón motor.
Biofeedback y condicionamiento operante
El condicionamiento operante es la base del aprendizaje basado en el ensayo-error, de tal manera que cualquier recompensa puede ser utilizada para reforzar inmediatamente cualquier respuesta que se ha emitido.
El biofeedback es muy similar en su metodología al condicionamiento operante, hasta el punto de ser considerado una prolongación del mismo, ya que el registro de una actividad fisiológica (en nuestro caso la contracción muscular) es llevado a un aparato de monitorización que transmite la variable medida y la devuelve (feedback) de tal forma que facilita el control de dicha variable fisiológica (fig. 2).

Fig. 2 Similitud entre el biofeedback y el condicionamiento operante
El biofeedback requiere que un estímulo exteroceptivo sea contingente con la actividad monitorizada, acompañándola; este estímulo puede ser un sonido, una luz, una gráfica o una animación en la pantalla del ordenador, etc…
Técnicas de condicionamiento operante en biofeedback
Los principios básicos del condicionamiento en biofeedback son:
- Reforzamiento: Se define como toda acción que aumenta (positivo) o disminuye (negativo o inhibitorio) la frecuencia de la respuesta. En lo aparatos de biofeedback, el feedback que se provee al paciente funciona como un reforzador secundario, ya que su presentación (luces, sonidos, gráficas en la pantalla del ordenador, etc…) tienen poco valor intrínseco, pero adquieren valor cuando el paciente establece la conexión del feedback con la mejora de su sintomatología; para ello es necesario, al inicio de la terapia, crear ese nexo, motivando al paciente por medio de elogios cada vez que consiga mejorar su ejecución bioinformativa.
- Programas de reforzamiento: Para adquirir y mantener el control de la conducta es necesario realizar un programa estructurado de distribución de esfuerzos. Al prncipio, se aplicará un feedback contínuo, que se presenta únicamente si se consigue la meta propuesta. Una vez que el paciente adquiere el dominio de la conducta, se realiza un reforzamiento intermitente, es decir, el feedback se produce cuando el paciente ha emitido varias respuestas, y no después de cada una de ellas; gradualmente se le irán pidiendo más respuestas antes de proporcionarle el feedback, de este modo se intenta conseguir la modificación permanente de la conducta sin necesidad del aparato de biofeedback.
- Modelado: Consiste en la presentación de respuestas sucesivas que se asemejen cada vez más a la deseada, para ello se establecen umbrales que el paciente debe intentar alcanzar.
- Generalización: Es la lógica extensión del modelado; consiste en la transferencia del estímulo a otros distintos a aquellos con los que se hizo el entrenamiento. Lo más frecuente es que es paciente extienda el control de la conducta, de la sala de tratamiento a las actividades de su vida diaria, primero mediante el control proporcionado por un dispositivo portátil de biofeedback y, finalmente, sin necesidad del mismo; otra opción es que el cambio de actividad en el músculo trabajado, se extienda a músculos cercanos, con lo que la función global mejora significativamente.
Utilización de la imagen mental
Para conseguir modificar la impronta neurológica y mejorar la sintomatología del paciente, es necesario conseguir una activación cerebral previa, es decir, se le pide al paciente que intente imaginar la actividad que luego va a tener que ejecutar, este proceso preactiva a casi todas las áreas cerebrales que van a intervenir cuando se ejecute reálmente la acción; de hecho, este paso previo provoca cambios en el registro electromiográfico.
Este proceso de creacción de una imagen mental de la actividad involucra fundamentalmente a tres procesos:
- Creación de una imagen visual: le pedimos que imagine una situación (p. ejm. está tumbado en la playa).
- Creación de una imagen somestésica: le pedimos que imagine las sensaciones que se producen en esa situación (p. ejm. imagina el calor del sol en la playa).
- Creación de una imagen motora: le pedimos que imagine un movimiento (p. ejm. estira los brazos).
Según el tipo de afectación, usamos con el paciente diferentes modalidades de evocación:
- Imaginar un movimiento con una articulación determinada en la zona afectada.
- Imaginar un movimiento primero en el lado no afecto.
- Imaginar sensaciones en el lado afecto.
- Mediante una transformación (fig. 3) visual-somestésica (imagen motora virtual o pura); se le pide al paciente que imagine un gesto copmplejo que se le presenta en fotografía (producción) o que describa ese gesto (decodificación).

Fig. 3 Las transformaciones
PRINCIPIOS DE APLICACIÓn EN LA HEMIPLEGIA
La hemiplegia es la alteración de la respuesta motora al medio, causada por una lesión cerebral caracterizada por una disfunción del tono en el hemicuerpo, que imposibilita o disminuye la ejecución del movimiento normal.
Los pacientes presentan diferentes afectaciones dependiendo del grado de lesión neurológica padecida. A nivel motor se produce una disfunción motora en diversas áreas y grados; además, si implica al hemisferio cerebral izquierdo, suele producir una afectación del área del lenguaje y, si es muy extensa, puede afectar a las funciones cognitivas (atención, memoria, conexión con el entorno, etc…) todo lo cual dificulta el uso del biofeedback electromiográfico.
En el daño cerebral adquirido se producen, básicamente, tres tipos de alteraciones: déficit sensitivo, hipotonía muscular e hipertonía muscular.
Déficit sensitivo
La disminución del feedback sensorial produce, de modo primario, una disminución de la capacidad del canal del feedback de retorno de la información sobre el sistema muscular (fig. 4).

Fig.4 Esquema de la disminución de la capacidad de transmisión de la información sensorial
El tratamiento con biofeedback electromiográfico consiste en complementar el canal alterado aumentando exteroceptívamente la capacidad disminuida de la vía sensorial (fig. 5).

Fig. 5 Esquema de tratamiento de la disminución de la información sensorial
Hipotonía muscular
La causa de la hipotonía suele ser, en principio, debida a la disminución o inactividad del canal sensorial de feedback que incide en la reducción de la actividad motora (fig. 6).

Fig.6 Esquema de la hipotonía muscular
El biofeedback electromiográfico, al reforzar la actividad sensorial, aumenta la actividad motora, que es detectada por la monitorización y devuelta al sujeto, incrementándose la actividad muscular (fig. 7).

Fig.7 Esquema del tratamiento de la hipotonía muscular
Hipertonía muscular
En la hipertonía muscular, así como en su máximo exponente, la espasticidad-rigidez, se produce una sobreactividad de la vía motora y sensorial, potenciándo un círculo vicioso (fig. 8).

Fig. 8 Esquema de la hipertonía muscular
Por medio del biofeedback electromiográfico, podemos incidir en la actividad sensorial, proveyendo de un feedback negativo para reducir la sobreactividad muscular, consiguiéndose que el paciente sea menos reactivo a los estímulos, y tenga un mayor control neuromuscular (fig. 9).

Fig. 9 Esquema del tratamiento de la hipertonía muscular
En relación al tratamiento con biofeedback electromiográfico, nos centraremos en la hipotonía y en la hipertonía. La hipotonía se manifiesta como una disminución del uso del sistema neuromuscular, y la hipertonía se manifiesta, bién como hipertonía en reposo, bién como sobreactividad muscular que dificulta el movimiento coordinado.
El biofeedback tiene como misión detectar y mostrar la función residual que, de otra manera, no es reconocida, para que el paciente la desarrolle; en los casos más frecuentes, donde la sintomatología principal es la debida a la hipertonía, el objetivo del tratamiento es atenuarla cuando se presente y, posteriormente, facilitar el movimiento.
CASO CLÍNICO
Paciente, diagnosticada de ICTUS hemiprotuberancial izqdo de etiologia indeterminada, con el resultado de hemiparesia dcho; el episodio ocurrió el 2/7/09.
Se evalúa la A.V.D. de alimentación en la actividad de alcanzar un vaso y levantarlo para llevarlo a la boca y beber, depositándolo a acontinuación en la mesa; la actividad se realiza en sedestación, con el vaso lleno de agua en 1/3 para añadirle peso, delante de la paciente a unos 60 cm frontal al ms dcho.
La duracion total de la actividad es de unos 18 sg con el siguiente desglose: fase 1, alcance y prensión del vaso unos 5 sg, fase 2, llevar el vaso a los labios 8 sg y fase 3, depositarlo de nuevo en la mesa 5 sg.
En la valoración visual, se observa como la paciente avanza el brazo derecho en abduccion de hombro de unos 50º con rotación interna de 90º, con el codo flexionado unos 90º en pronación y con la muñeca en leve flexión dorsal, con desviación radial y los dedos semiflexionados en ráfaga cubital. A nivel del hombro, se aprecia como activa de modo inmediato el trapecio superior, con elevación del muñón del hombro y arrastre de la escápula en rotación externa, al no ser estabilizada por el trapecio inferior; para compensar esto junto a la debilidad del deltoides anterior (insuficiente para elevar el brazo), la paciente inclina el tronco y la cabeza a la izquierda compensando asi la limitación de la amplitud articular a nivel de la glenohumeral, necesaria para realizar la actividad de forma efectiva.
Se opta por valorar y tratar la primera fase (alcance y elevación, durante unos 5-4 sg, del vaso a unos 10 cm sobre la mesa) ya que es donde se observan las mayores suplencias por parte de la paciente (fig 10).
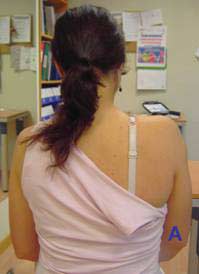
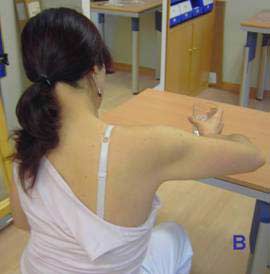
Fig. 10 Secuencia de inicio (A) y final (B) de la primera fase
Valoración electromiográfica inicial
En la realización del presente estudio se ha utilizado el aparato de biofeedback electromiográfico “Neurotrac ETS” con el correspondiente software, versión 3.01. Para realizar las valoraciones electromiográficas se han usado electrodos de corchete con los correspondientes cables adaptadores (fig. 11), mientras que para las sesiones de tratamiento en modo ETS se utilizaron electrodos de gel recortados con unas medidas aproximadas de 2.5 X 2.5 cm.
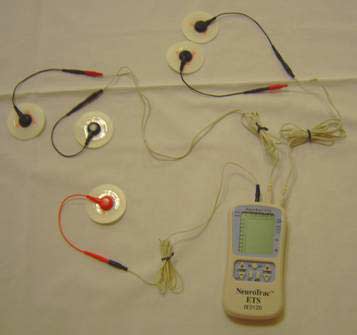
Fig. 11 Neurotrac ETS y electrodos de corchete con adaptadores
Se decide monitorizar mediante E.M.G. los músculos del brazo derecho implicados en esta primera fase de la actividad: trapecio superior (excesivamente activo desde un primer momento) en el canal B y trapecio inferior (insuficiente para estabilizar la escapula) en el canal A. Los electrodos se colocan según criterios de la S.E.N.I.A.M. (Surface Electromiography for the Non-Invasive Assessment of Muscles), lo más junto posible entre sí, en el centro de las líneas que unen T8 con el trigonum spinea (trapecio inferior) y C7 con el acromion (trapecio superior), el electrodo de referencia se coloca en la clavícula izquierda (fig. 12).
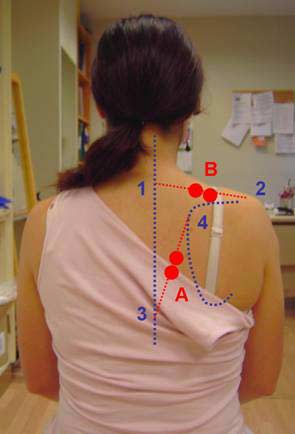
Fig. 12 Aplicación de los electrodos de registro del trapecio inferior (A) y del superior (B)
1 C7, 2 acromion, 3, T8, 4 trigonum spinea
Los parámetros analizados son los siguientes (fig. 13):
- Valor medio de la línea de base: Representa el valor promedio de actividad, en µV, del músculo en reposo; en el músculo sano suele ser de unos -10 µV.
- Valor umbral medio: Representa el valor medio de la intensidades de la contracciones de mejor calidad.
- Dispersión: Representa la aparición de oscilaciones en las intensidad de la contracción; su aumento indica la fatiga muscular creciente y que la actividad debe cesar. Para calcularla se toma la diferencia entre los picos máximo y mínimo del segmento de la contracción de mejor calidad, es decir, donde la dispersión aún no ha aumentado excesívamente.
- Actividad fásica: Es la que aparece al realizar una contracción brusca e intensa, generando una curva en forma de pico de una duración aproximada de 1 sg en el músculo sano.
- Actividad tónica: es la que aparece en la mayoría de las actividades de la vida diaria, generando una curva con meseta estable.
- Factor de correlación agonista-antagonista: Representa la proporción entre la intensidad de contracción de un músculo y su antagonista en una actividad. Suele ser de 3 normálmente, es decir, la intensidad de contracción del agonista es tres veces mayor que la del antagonista.
- End Plate Potential (E.P.P.): Es el punto de arranque de la contracción que debe coincidir con el momento en que se da la orden de realizarla. En los paciente con daños neurológicos suele estar retrasado, de modo que genera la contracción más tarde que la orden de realizarla.
- Electro-Mechanical Delay (E.M.D.): Es la velocidad con la que el músculo se activa y desactiva. Normálmente esta velocidad suele ser muy alta, de modo que las pendientes de ascenso y descenso de la curva son muy verticales.
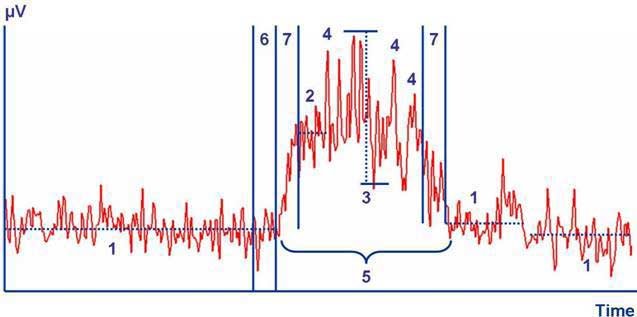
Fig. 13 Parámetros analizados: 1 línea de base, 2 valor umbral de mejor calidad,
3 dispersión, 4 picos fásicos, 5 actividad tónica, 6 E.P.P . 7 E.M.D.
Durante la prueba, se le solicita al paciente que realice una inspiración profunda que, normálmente, no debería modificar excesívamente el registro. Seguídamente se le pide que realice la actividad varias veces hasta que se observe un aumento significativo en la dispersión, lo cual indica el agotamiento muscular; con esta prueba determinamos, además de los parámetros anteriores, el número óptimo de repeticiones sín que aparezca dispersión, así como el tiempo óptimo de descanso para que la línea de base recupere la normalidad.
En la prueba resultante se observa como en la línea de base inicial, no hay alteraciones de la misma con la sinergia respiratoria y la duración del E.P.P. es mínima en todas las repeticiones; el valor medio de la línea de base del trapecio inferior es de unos 24 µV con una dispersión de unos 20 µV (83% del valor umbral medio); el valor medio de la línea de base del trapecio superior es de unos 15 µV con una dispersión de unos 18 µV (120% sobre el umbral medio). El E.M.D. de la fase tónica es de 1.5 sg en el inicio aumentando en la finalizacion de la actividad, con dificultades para relajar ambos musculos; en el trapecio inferior, se observa como la fase tónica de mejor calidad dura 4 sg, con aumento posterior de la dispersión, su valor medio sube de 39 a 43 µV a medida que la potencia de la contracción aumenta, con un valor medio de unos 41 mV y una dispersión de 29 µV (70% del valor umbral medio); en el trapecio superior, la dispersión durante toda la actividad es en general mayor, incluso con picos fásicos en el periodo central, tras el cual, su actividad decrece por agotamiento aunque aun no ha terminado la actividad, durante los primeros 4 sg, el valor medio es de unos 34 µV y la la dispersión es de unos 28 µV (82% del valor umbral medio). El factor de correlacion entre ambos durante la actividad es de 1.2. A partir de la tercera repetición, la dispersión se va acentuando en ambos músculos por agotamiento (incluso con picos fásicos muy pronunciados en el trapecio superior), además de observar una aumento del E.M.D. tanto para iniciar la actividad, como para terminarla y reducir el valor de la línea de base a valores de reposo, con problemas cada vez mayores en esta última fase, mientras que el valor umbral medio permanece más o menos constante. La línea de base interfase, disminuye progresivamente, desde los 24 µV iniciales a 12 µV al final en el trapecio inferior y desde los 15 µV iniciales del trapecio superior hasta 11 µV al final, con un factor de correlación que disminuye también hasta ser al final de prácticamente 1 (fig. 14).
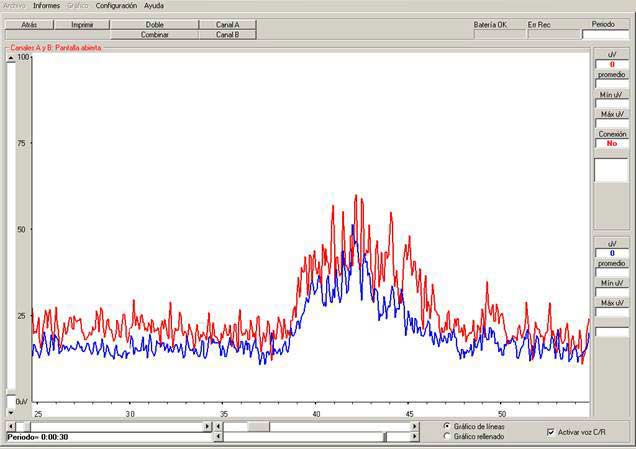
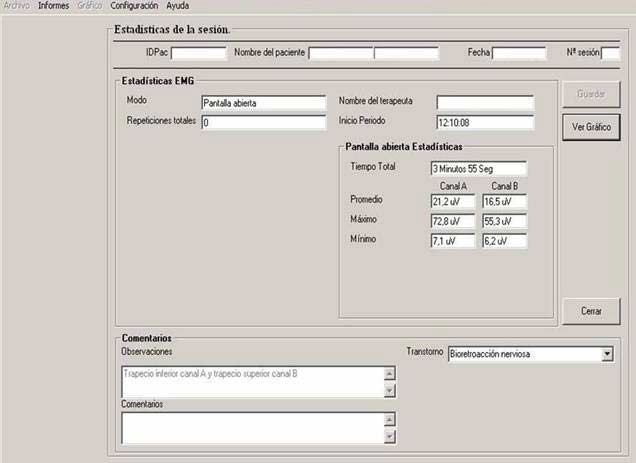
Fig. 14 Valoración E.M.G. trapecio superior (canal B azul) y trapecio inferior (canal A rojo) Gráfica y estadísticas de la sesión
Metodología de tratamiento
El planteamiento inicial va a ser el de mejorar la estabilidad de la escapula durante la actividad, lo que implica un control inhibitorio del trapecio superior (por eso lo monitorizamos en el canal B) y la mejora de la actividad del trapecio inferior (por eso lo monitorizamos en el canal A), de este modo se espera mejorar la alineación del tronco y facilitar al deltoides durante la realización de la actividad.
Para conseguir este objetivo se va a entrenar la primera fase de la actividad descrita con control E.M.G. del trapecio superior e inferior; en el superior se establecerá un feedback inhibitorio sonoro con el umbral a 32 µV. Dado el factor de correlación de 1.2, en el trapecio inferior se trabajara en modo E.T.S. con activación de la fase STIM a un umbral de 41 µV, con 1 sg de demora y durante 3 sg. En ambos músculos se establecerá como tiempo de trabajo 4 sg, es decir, durante el periodo de alcance y sostén en el aire del vaso, considerándose como fase de reposo el tiempo que tarde en depositar de nuevo el vaso en la mesa (5 sg) asi como el periodo interfase de recuperación (40 sg), con un total de 45 sg de tiempo de reposo. Se realizarán 2 repeticiones ya que, tal como se ha descrito, la fatiga hace que la calidad de las mismas empeore rápidamente.
Los parámetros programados en el modo STIM para el trapecio inferior (canal A), cuya actividad queremos mejorar, son los siguientes:
- RATE 40 Hz (trabajo de fibras tónicas mixtas).
- WDTH 450 μsg de anchura de pulso.
- WORK 3 sg (duracion de la actividad “coger el vaso y sostenerlo”).
- REST 45 sg (5 sg para depositar el vaso y 40 sg de reposo).
- MINS 002, para dar tiempo a 2 repeticiones.
- RAMP 9.9 ya que es una actividad funcional que requiere de un periodo relatívamente largo para ser ejecutada.
- OFF CHB ya que no vamos a estimular el trapecio superior.
Los parámetros programados en el modo ETS son los siguientes:
- VOL 10 para sumar feedback auditivo.
- WORK 4 sg ya que es la duración estimada de la actividad “coger el vaso y sostenerlo en el aire”.
- REST 45 sg coincidiendo con el modo STIM.
- TRLS 02, es decir, dos repeticiones como en el modo STIM.
- ABV FDBK para activar la electroestimulación en el trapecio inferior al superar el umbral de 41 µV.
- ON SDAT para trabajar con el ordenador en el modo “Controlado por el Neurotrac”.
- OFF AUTO, ya que ajustamos el umbral manualmente; para trabajar a domicilio, una vez entrenado al paciente, si que lo pondríamos en el modo ON AUTO.
- ELDT 01 para que el modo STIM en el trapecio inferior se active en cuanto se alcance el umbral de 41 µV (el tiempo mínimo de demora es de 1 sg).
- NRW FLTA, banda estrecha en el canal A.
- ON CHB para activar el canal B, el del trapecio superior.
- NRW FLTB, banda estrecha en el canal B.
- ON FBIH, activamos el feedback inhibitorio en el trapecio superior (canal B) ya que el objetivo es mantenerlo con un tono bajo durante la ejecución de la actividad.
- CBTH 032 μV de umbral inhibitorio en el canal B, de este modo intentamos que el trapecio superior mantenga una actividad baja.
- THRS 41 μV de umbral de activación de la fase STIM en el trapecio inferior (canal A).
En el modo ETS, el valor umbral necesario para activar el modo STIM se modifica manualmente en cada sesión, adaptándolo a la actividad que presente el paciente; para trabajo domiciliario, se ajusta en modo automático, de manera que el propio “Neurotrac” ajuste el umbral a las variaciones que se produzcan el en registro E.M.G (Fig. 15). Respecto a la intensidad de la electroestimulación, su valor se ajusta manualmente al inicio de cada sesión, siendo necesarios 37-40 mA para provocar contracción franca del trapecio inferior.
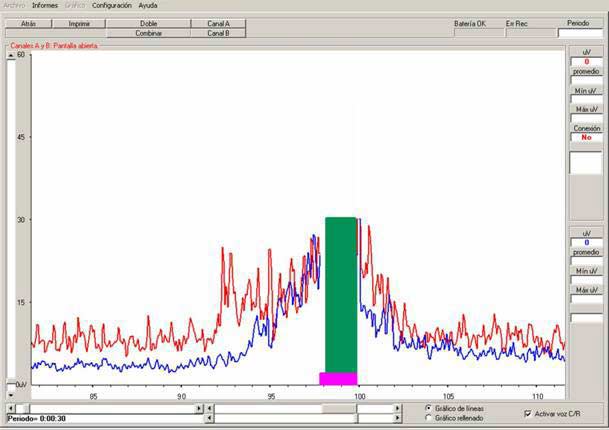
Fig. 15 Ejemplo de trabajo en modo ETS
Previo a la sesión con B.F.B. se entrenará el gesto de descenso y posteriorización del muñon del hombro dcho, actividad que implica precísamente la activación del trapecio inferior y un tono bajo en el trapecio superior; para ello se va a usar el patrón de P.N.F. de descenso con rotación interna de la escapula (fig. 16), usando las técnicas de iniciación rítmica libre primero, con un set de tres repeticiones, seguido de un set de tres repeticiones con resistencia, y finalizando con la ejecución del gesto “coger el vaso y levantarlo de la mesa” con activación previa y mantenida todo el tiempo del descenso del hombro, también con un set de tres repeticiones.
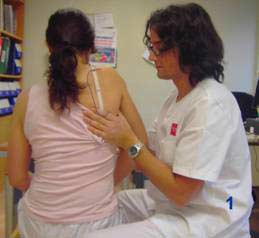
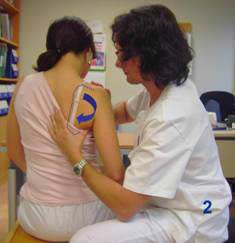
Fig. 16 Patrón P.N.F. de descenso con rotación interna de la escápula
1 posición inicial, 2 posición final
El esquema de trabajo consistirá en dos sesiones de B.F.B. precedidas del trabajo descrito en el párrafo anterior y con un descanso de 10 minutos entre ambas. El tratamiento se ha realizado durante 4 días.
Valoración electromiográfica final
En la última valoración se observa como en la línea de base inicial, sigue sin haber alteraciones de la misma con la sinergia respiratoria y la duración del E.P.P. también sigue siendo mínima en todas las repeticiones; el valor medio de la línea de base del trapecio inferior ha descendido a solo 7 µV así como la dispersión, que es de unos 7 µV (100% del valor umbral medio); el valor medio de la línea de base del trapecio superior también ha descendido a solo 3 µV con una dispersión de solo 2 µV (66% sobre el umbral medio). El E.M.D. se ha reducido a menos de 1 sg en el inicio de la actividad, aunque sigue alargándose en la finalización de la misma, con dificultades para relajar ambos musculos; en el trapecio inferior, se observa como la fase tónica de mejor calidad dura 2-3 sg, con aumento posterior de la dispersión, su valor medio ha descendido a 21 µV y la dispersión a 9 µV (42% del valor umbral medio); en el trapecio superior, la dispersión durante toda la actividad es en general mayor, persistiendo los picos fásicos en el periodo central, ain embargo, no se agota y mantiene su actividad todo el tiempo, durante la primera fase, suvalor medio es de solo 17 µV y la dispersión de 8 µV (47% del valor umbral medio). El factor de correlacion entre ambos sigue siendo de 1.2. En las siguientes repeticiones, los valores permanecen constantes evidenciándose un aumento de la dispersión y del E.M.D. en la cuarta repetición (Fig. 17).
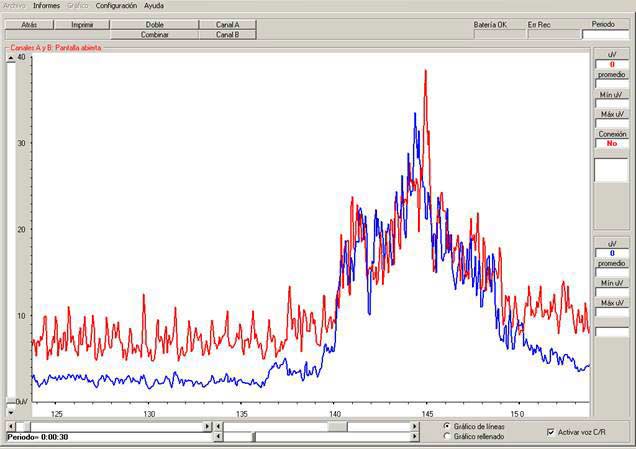
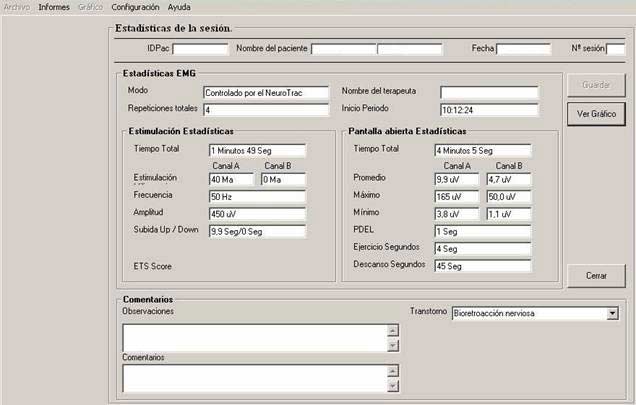
Fig. 17 Valoración E.M.G. trapecio superior (canal B azul) y trapecio inferior (canal A rojo) Gráfica y estadísticas de la sesión
ANÁLISIS DE LOS RESULTADOS
Como se deduce del análisis del registro E.M.G. en solo cuatro sesiones de tratamiento se ha producido una mejora significativa en el patrón de activación muscular durante el gesto “alcance y sostén del vaso sobre la mesa”.
En general, la actividad de ambos músculos durante el gesto se ha reducido en un 50%, mientras que en reposo, esta reducción llega a ser de un 71% en el trapecio inferior y de un 80% en el trapecio superior. De manera simultánea, la dispersión también ha disminuido de intensidad en un 70% para ambos músculos durante la actividad, mientras que, en reposo, la reducción es de un 65% en el trapecio inferior y de hasta un 90% en el trapecio superior.; sin embargo, en valores porcentuales, la dispersión no ha sufrido modificaciones tan grandes, de ahí que la forma del registro es similar, tanto en la valoración inicial como en la final, aún así, se ha reducido en un 30% en ambos músculos durante la actividad y, si bién en reposo aumenta discrétamente en el trapecio inferior (probablemente de modo secundario a la estimulación), en el trapecio superior se ha reducido en un 40%. Asimismo, el valor del E.M.D. de activación ha pasado de 1.5 sg a menos de 1 sg, mientras que el factor de correlación se mantiene constante en 1.2 (Fig. 18).
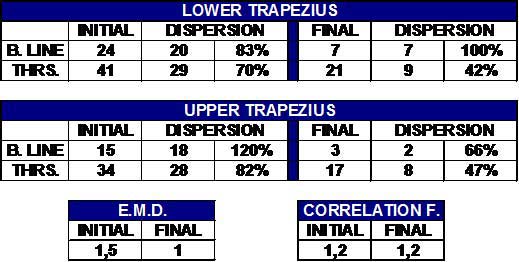
Fig. 18 Análisis de los resultados
CONCLUSIÓN
como hemos mencionado, solo cuatro sesiones han sido necesarias para reducir la intensidad y, por tanto, el gasto energético muscular durante la actividad; asimismo, el tono de base en reposo de ambos músculos se ha reducido siendo especiálmente significativa en el trapecio superior; todo ello evidencia como, usando el biofeedback E.M.G. se ha reducido de modo muy rápido el nivel de actividad muscular, sobre todo en el trapecio superior, que interfería en el gesto. Por otro lado, la reducción del E.M.D. también evidencia un reclutamiento más rápido de las unidades motoras y una mejora en la velocidad de respuesta.
Por el contrario, aunque disminuida, la dispersión, en valores porcentuales, sigue siendo alta; el factor de correlación tampoco ha aumentado, como sería deseable, lo que indica que serían necesarias un número mayor de sesiones para modificar estos parámetros.
Bibliografía
- www.seniam.org
- Woodford H, Price C (2007) EMG biofeedback for the recovery of motor function after stroke.Cochrane Database Syst Rev.Apr 18;(2):CD004585.
- Ottawa Panel, Khadilkar A, Phillips K, Jean N, Lamothe C, Milne S, Sarnecka J (2006). Ottawa panel evidence-based clinical practice guidelines for post-stroke rehabilitation.Top Stroke Rehabil.Spring;13(2):1-269.
- Van Peppen RP, Kwakkel G, Wood-Dauphinee S, Hendriks HJ, Van der Wees PJ, Dekker J (2004) The impact of physical therapy on functional outcomes after stroke: what's the evidence?Clin Rehabil.Dec;18(8):833-62.
- Cram JR Durie MD (in press) The history of muscle disfunction and SEMGJournal of Applied Phsycophysiology and BiofeedbackRetrieved February 28, from www.semg.org
- Several authors. (2002) National clinical guidelines for stroke: a concise update.Clin Med.May-Jun;2(3):231-3.
- Snels IA, Dekker JH, van der Lee JH, Lankhorst GJ, Beckerman H, Bouter LM (2002) Treating patients with hemiplegic shoulder pain.Am J Phys Med Rehabil.Feb;81(2):150-60.
- Medved V (2001)Measurement of human locomotion, Boca Raton, FL, CRC Press.
- Kleissen RFM, Buurke JH, Harlaar J, Zilvold G (1998) Electromiography in the biomechanical analysis of human movement and it´s clinical applicationGait and Posture8, 143-158.
- De Luca CJ (1997) The use of surface electromyography in biomechanicsJournal of Applied Biomechanic,13, 135-165.
- Stálberg E, Nandedkar S, Sanders D, Falk B (1996) Quantitative Motor Unit Potential Analysis.J Clin Neurophysiol 13: 401‑26.
- Several authors (1996) AAEM. Guidelines es for Establishing a Quality Asssurance Program in an Electrodiagnostic Laboratory.Muscle Nerve19: 1496‑1502.
- Shields RW (ed) (1995). Motor unit number estimation.J. Clinical Neurophsiol12: 537‑594.
- Clarys JP (1994) Electrology and localizated electrization revised,Journal of Electromiography and vendaje neuromuscularlogy4, 5-14.
- Hallett M, Beradelli A, Delwaide P, et al. (1994) Central EMG and tests of motor control. Report of the IFCN committee.EEG clin Neurophysiol90: 404‑432.
- Peroto A et al. (1994)Anatomical Guide for the Electromyographe,Springfield.
- DeLisa JA et al. (1994)Manual of Nerve Conduction Velocity and Clinical Neurophysiology,3TH edition, New York, Raven Press.
- Stálberg E, Trontej JV (1994)Single Fiber EMG,Raven Press.
- Hagbarth KE, Torebjörk E, Wallin BG (1993) Microelectrode explorations of human peripheral nerves. En Dyck PJ, Thomas PK.Peripheral Neuropathy.Vol l: 658‑671.
- Latash ML(1993)Control of human movement, Human Kinetics.
- Liveson JA (1992)Laboratoty Reference for Clinical Neurophysiology, FA Davis Co. Philadelphia.
- Murray NMF (1992) Motor Evoked Potentials.InElectrodiagnosis in Clinical Neurology, New York, Churchill Livingstone, 1992: 605‑626.
- Lindblom U, Ochoa JL (1992) Somatosensory Function and Dysfunction. In Asbury A,Mc Khan y Mc Donald IW (ed):Diseases of the Nervous System Vol 1:283‑98.
- Several authors (1992) American Association of Electrodiagnostic Medicine (AAEM). Guidelines in Electrodiagnostic Medicine.Muscle Nerve15: 229‑253.
- Fuglsang‑Frederiksen A, Ronager J (1990) EMG power spectrum, turn‑amplitude analysis and motor unit duration in neuromuscular diseases.J Neurol Sci97: 81‑90.
- Dorfman L, Howard J (1989) Clinical studies using automatic decomposition electromyography (ADEMG) in needle and surface EMG. In Desmedt JE (ed),Computer aided Electromyography and expert systems. Clinical neurophysiology,Amsterdam, Elsevier 1989: 189‑204.
- Stashut D, De Luca C (1989) Update on the decomposition electromyography: an analysis of the EMG signals. In Desmedt JE (ed)Computer aided Electromyography and expert systems. Clinical neurophysiology update,Amsterdam. Elsevier 1989: 39‑53.
- Kimura J (1989)Electrodiagnosis in diseases of the nerve and muscle. Principles and practice,Philadelphia, FA Davis.
- Loch G. E. Gans C (1986)Electromyography for experimentalists,Chicago, University of Chicago Press.
- Trontej JV, Mihelin M, Fernández JM, Stálberg E (1986) Axonal stimulation for end‑plate jitter studies.J Neurol Neurosurg Psychiatry46: 677‑85.
- Stálberg E (1983) AAEM minimonograph.Muscle and Nerve6: 619‑30.
- Basmajian JV (1981) Biofeedback in rehabilitation: a review of principles and practices.Arch Phys Med Rehabil.Oct;62(10):469-75.
- Basmajian JV (1978)Muscles alive: their function revealed by electromyography, 4TH edition, Baltimore, Wiliams and Wilkins.
- Aminoff MJ (1978)Electromiography in clinical practice,Mento Pack, CA, Addison-Wesley Publishing.
- Basmajian JV, Regenos EM, Baker MP. (1977) Rehabilitating stroke patients with biofeedback.Geriatrics.Jul;32(7):85-8.
- Lee KH, Hill E, Johnston R, Smiehorowski T. (1976) Myofeedback for muscle retraining in hemiplegic patients.Arch Phys Med RehabilDec;57(12):588-91.
- Licht S (1971) History of electrodiagnosis, In S. Licht (ed)Electrodiagnosis and electromyography,New Haven, CL, Elizabeth Licht Publisher, 1971.
- Basmajian J. V. Stecko G (1962) A new bipolar electrode for electromyographyJournal of Applied Physiology,17,849.
- Buchthal F (1957) AnIntroduction to Electromyography,Scandinavian University Books, Glydendal.
